Chapitre 11a : Structure et polarité des entités chimiques⚓︎
▶️ Capsule : Le cours complet
I - Le schéma de Lewis⚓︎
A savoir
1. Schéma de Lewis d’un atome⚓︎
Le schéma de Lewis d’un atome représente la couche électronique de valence de l’atome :
-
On établit la configuration électronique de l’atome.
-
On détermine le nombre d’électrons de valence (électrons de la couche de valence) : il correspond aussi au chiffre des unités du numéro de la colonne du tableau périodique où se trouve l’atome.
-
On répartit les électrons de valence, représentés par des ●, l’un après l’autre de chaque côté du symbole
-
Les électrons de valence qui :
- se retrouvent seuls sur un même côté constituent des électrons célibataires représenté par un point ●.
- se retrouvent par paires sur un même côté forment un doublet non liant représenté par un trait .

▶️ Capsule : Le schéma de Lewis des atomes
2. Schéma de Lewis d’un ion monoatomique⚓︎
Un ion monoatomique est un atome qui a gagné ou perdu un ou des électrons pour obtenir la configuration électronique du gaz noble le plus proche, et obtenir ainsi une couche externe saturée : le schéma de Lewis est le même que celui de l’atome correspondant auquel on enlève ou on rajoute le bon nombre d’électrons

▶️ Capsule : Schéma de Lewis des ions mono et polyatomiques
lewis_ion
3. Schéma de Lewis d’une molécule⚓︎
Le schéma de Lewis d’une molécule s’établit en assemblant les schémas de Lewis des atomes. Un atome forme autant de liaisons qu’il a d’électrons célibataires. On place d’abord l’atome central puis on lui associe les autres atomes : l’atome central est celui qui peut en former le plus de liaisons.
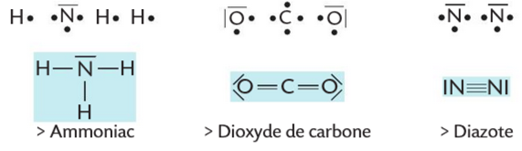
▶️ Capsule : Schéma de Lewis des molécules
3. Charge formelle d’un ion polyatomique⚓︎
Pour les ions, on détermine quel atome porte la charge formelle en comptant le nombre d’électrons propres de chaque atome et en le comparant au nombre d’électrons de l’atome isolé :
-
Si l’atome a un électron propre de moins qu’à l’état isolé, on lui attribue une charge positive + .
-
Si l’atome a un électron propre de plus qu’à l’état isolé, on lui attribue une charge négative - .
▶️ Capsule : Schéma de Lewis des ions mono et polyatomiques
lewis_ion
3. Lacune électronique⚓︎
Dans certaines entités, il arrive qu’un atome n’aie pas la configuration électronique du gaz noble le plus proche : il porte alors autant de lacunes électroniques que de doublets manquants. Une lacune est représentées par un petit rectangle ▯.
▶️ Capsule : Lacunes électroniques
II - Géométrie des entités⚓︎
A savoir
La théorie VSEPR, mise au point par le chimiste britannique Ronald Gillespie en 1957, permet de prédire la géométrie des molécules en partant d’un principe simple : les doublets d’électrons (liants ou non liants) autour d’un atome étant négatifs, ils se repoussent mutuellement et adoptent des directions qui leur permettent d’être au maximum éloignés les uns des autres.
Pour connaître la géométrie autour d’un atome, il faut compter le nombre de liaisons (doublets liants) et le nombre de doublets non liants autour de lui :
| Molécule | Schéma de Lewis | Configuration de l’atome central | Géométrie de doublets | Modèle | Géométrie de la moélcule |
|---|---|---|---|---|---|
| Méthane \(CH_4\) |
 |
C entouré de : 4 voisins |
 |
 |
Tétraèdrique |
| Ammoniac \(NH_3\) |
 |
N entouré de : 3 voisins 1 doublet non liant |
 |
 |
Pyramidale |
| Eau \(H_2O\) |
 |
O entouré de : 2 voisins 2 doublet non liants |
 |
 |
Coudée |
| Méthanal \(CH_2O\) |
 |
C entouré de : 3 voisins |
 |
 |
Trigonale (ou triangulaire) |
| Cyanure d'hydrogène \(HCN\) |
 |
N entouré de : 2 voisins |
 |
 |
Linéaire |
VSEPR signifie : « Valence Shell Electronic Pairs Repulsion », ce qui signifie : « Répulsion des Paires Electroniques de la couche de Valence. »
▶️ Capsule : Géométrie des molécules
▶️ Capsule : Déterminer la géométrie
III - Polarité des molécules⚓︎
A savoir
1. L'électonégativité⚓︎
L’électronégativité d’un élément chimique est une grandeur sans unité, désignée par la lettre grecque khi \(\chi\).
Elle représente la capacité d’un élément à attirer les électrons d’une liaison covalente : plus un élément chimique est électronégatif, et plus il attire les électrons.
Le fluor (en haut à droite) est l’élément le plus électronégatif. L’électronégativité augmente donc (sauf exceptions) de gauche à droite et de bas en haut.

2. Polarité d'une liaison⚓︎
Pour savoir si une liaison A-B est polarisée, on calcule la différence d’électronégativité \(\Delta\chi\) entre les deux atomes A et B impliqués dans la liaison :
Si \(\Delta\chi<=0,4\) alors la liaison est non polarisée ou apolaire : le doublet d’électrons est alors équitablement réparti entre les deux atomes.
Si \(\Delta\chi>0,4\) alors a liaison est polarisée : le doublet d’électrons de la liaison est plus proche de l’atome le plus électronégatif. On ajoute une charge partielle \(\delta^-\) sur l’atome le plus électronégatif et une charge partielle \(\delta^+\) au-dessus de l’atome le moins électronégatif.

3. Polarité d'une molécule⚓︎
▶️ Capsule : Polarité d’une molécule
Une molécule est dite polaire les deux conditions suivantes sont respectées :
- elle contient au moins une liaison polarisée.
- le « centre géométrique » des charges positives (noté \(G^+\)) est différent du centre géométrique des charges négatives (noté \(G^-\))
Une molécule est dite apolaire si :
- il y a des liaisons polarisées et que les deux centres \(G^+\) et \(G^-\) sont confondus.
- Il n’y a aucune liaison polarisée.

▶️ Capsule : Déterminer la polarité exemple 1
▶️ Capsule : Déterminer la polarité exemple 2