Chapitre 4 : Composition des solutions⚓︎
I - Préparation d'une solution⚓︎
A savoir
Protocole de la dissolution⚓︎
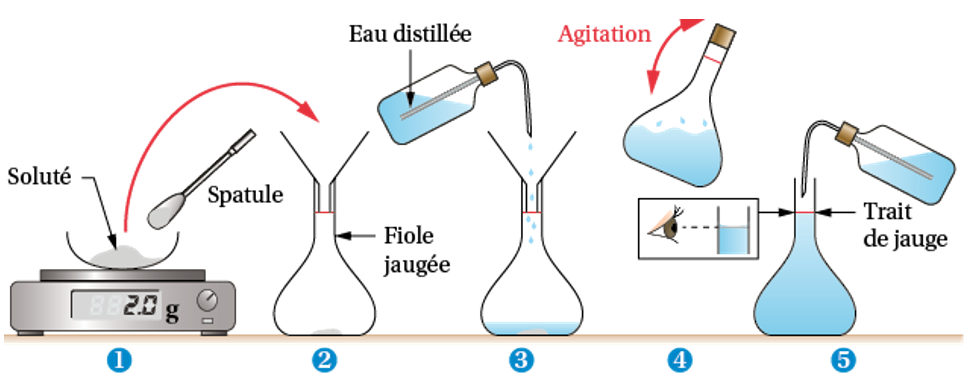
Protocole de la dilution⚓︎
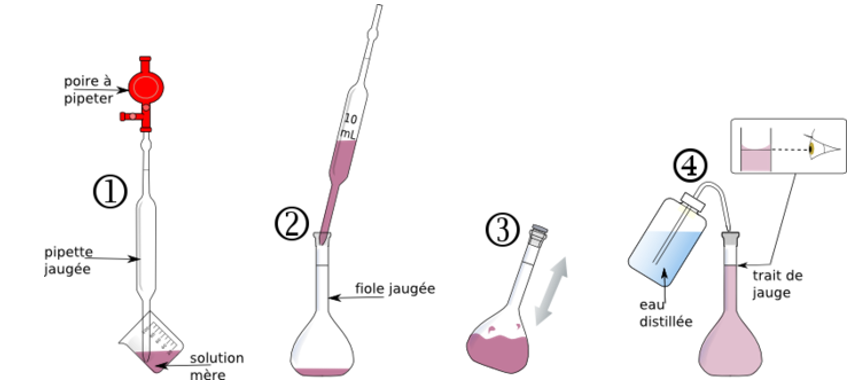
II - Absorbance et loi de Beer-Lambert⚓︎
A savoir
L'absorbance A d'une solution est une grandeur sans unité qui mesure la capacité d’une solution à absorber la lumière qui la traverse pour une longueur d’onde \(\lambda\) donnée.
Pour mesurer l'absorbance, on place la solution dans la cuve d'un spectrophotomètre ou d’un colorimètre.
Pour une longueur d’onde donnée \(\lambda\) , l'absorbance d’une solution de faible concentration est proportionnelle à la concentration molaire en espèce colorée de la solution : c’est la loi de Beer-Lambert.
k est une constante qui dépend :
- de l'espèce chimique considérée par son coefficient d'absorption molaire \(\varepsilon\).
- de la longueur \(l\) de solution traversée.
III - Couleur d’une solution : la spectroscopie UV-Visible⚓︎
A savoir
Si on mesure l’absorption d’une solution contenant une espèce chimique colorée en faisant varier la longueur d’onde λ on obtient le spectre d’absorption de cette espèce chimique en solution : ce spectre peut être tracé en utilisant les domaines de radiations UV-Visible.
Si le spectre d’absorption présente un maximum d’absorption dans les radiations visibles alors la couleur de la solution est la couleur complémentaire de celle des radiations absorbées qui peut être déterminée à partir du cercle chromatique.
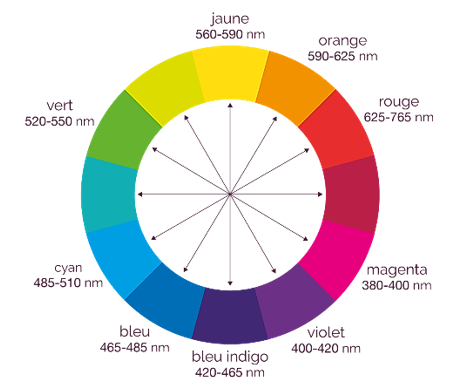
Exemple
Le spectre de la solution de permanganate de potassium ci-dessous présente un maximum d’absorption autour de 535nm donc pour les radiations vertes.
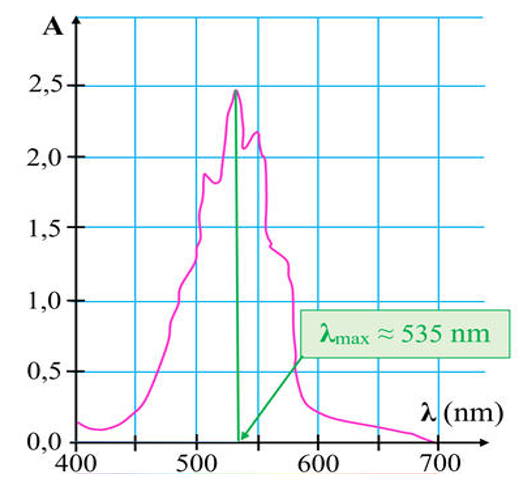
La couleur de la solution correspond donc à la couleur complémentaire sur le cercle chromatique soit le magenta (rose-violet).
IV - Dosage par étalonnage spectrophotométrique⚓︎
A savoir
Doser une espèce chimique consiste à déterminer sa concentration (molaire ou massique) dans une solution.
Le dosage par étalonnage consiste à mesurer une grandeur physique qui dépend de la concentration C de l’espèce étudiée.
Lors d’un dosage par étalonnage spectrophotométrique la grandeur physique mesurée est l’absorbance A de la solution.
va donc chercher à obtenir la courbe d’étalonnage A = f(C) afin de déterminer la concentration d’une solution inconnue.
Les mesures sont toutes faites pour la longueur d’onde \(\lambda_{max}\) qui permet l’absorbance maximale.
| La démarche expérimentale est la suivante | |
|---|---|
| Etape 1: | |
| Choisir ou fabriquer une gamme de solutions dites « étalons » de concentrations connues préparées par dilution d’une solution mère. |  |
| Etape 2: | |
| Mesurer l’absorbance choisie pour chaque solution. | 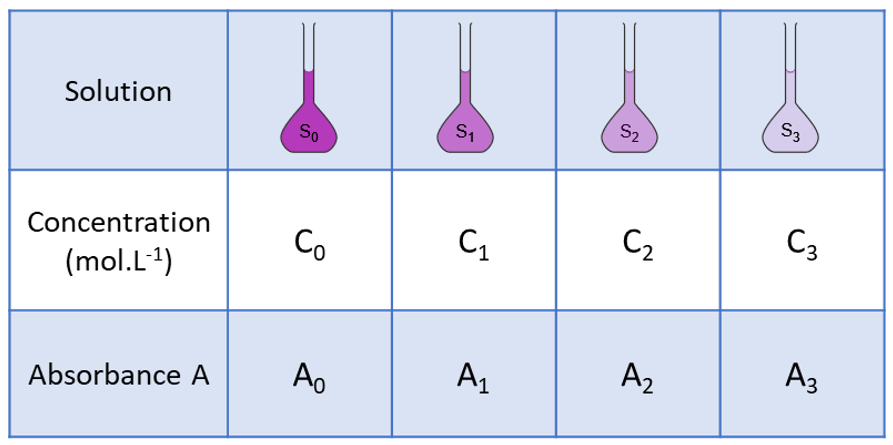 |
| Etape 3: | |
| Tracer la courbe d’étalonnage de l’absorbance en fonction de la concentration \(A = f(C)\). | 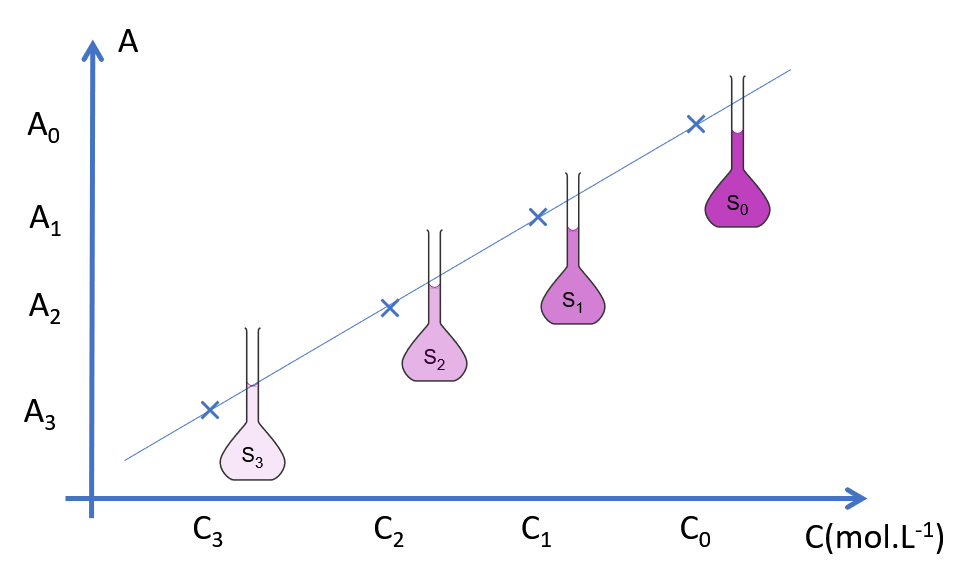 |
| Etape 4: | |
| Mesurer l’absorbance pour l’échantillon inconnu. | 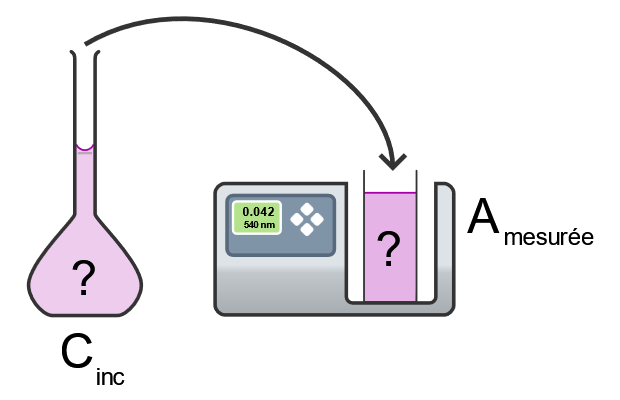 |
| Etape 5: | |
| Reporter cette valeur sur la courbe pour en déduire sa concentration. | 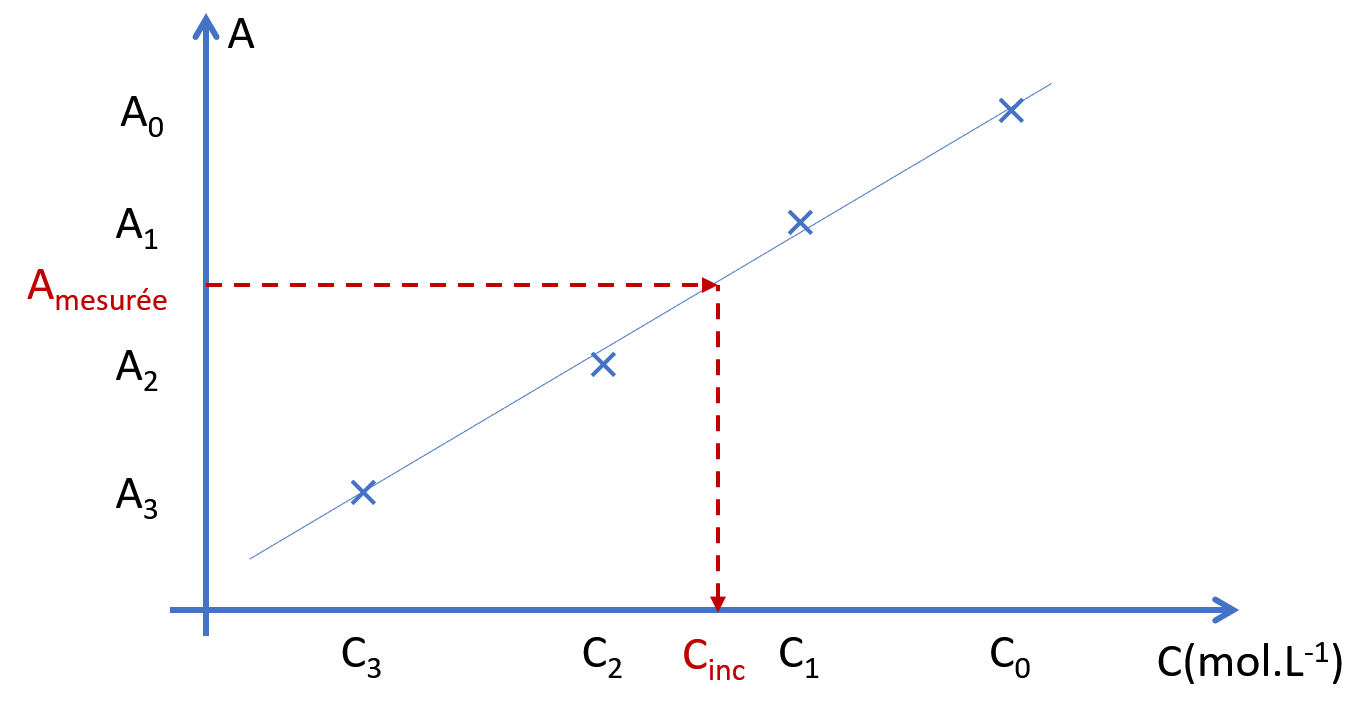 |