Chapitre 6 : Oxydoréduction et avancement⚓︎
I - Oxydant, réducteur et demi-équation électronique⚓︎
A savoir
1. Vocabulaire⚓︎
Un oxydant est une espèce chimique susceptible de capter un ou plusieurs électrons.
Un réducteur est une espèce chimique susceptible de céder un ou plusieurs électrons.
Un oxydant et son réducteur conjugué forment un couple oxydant/réducteur (toujours notés dans cet ordre) lié par une demi-équation électronique telle que :
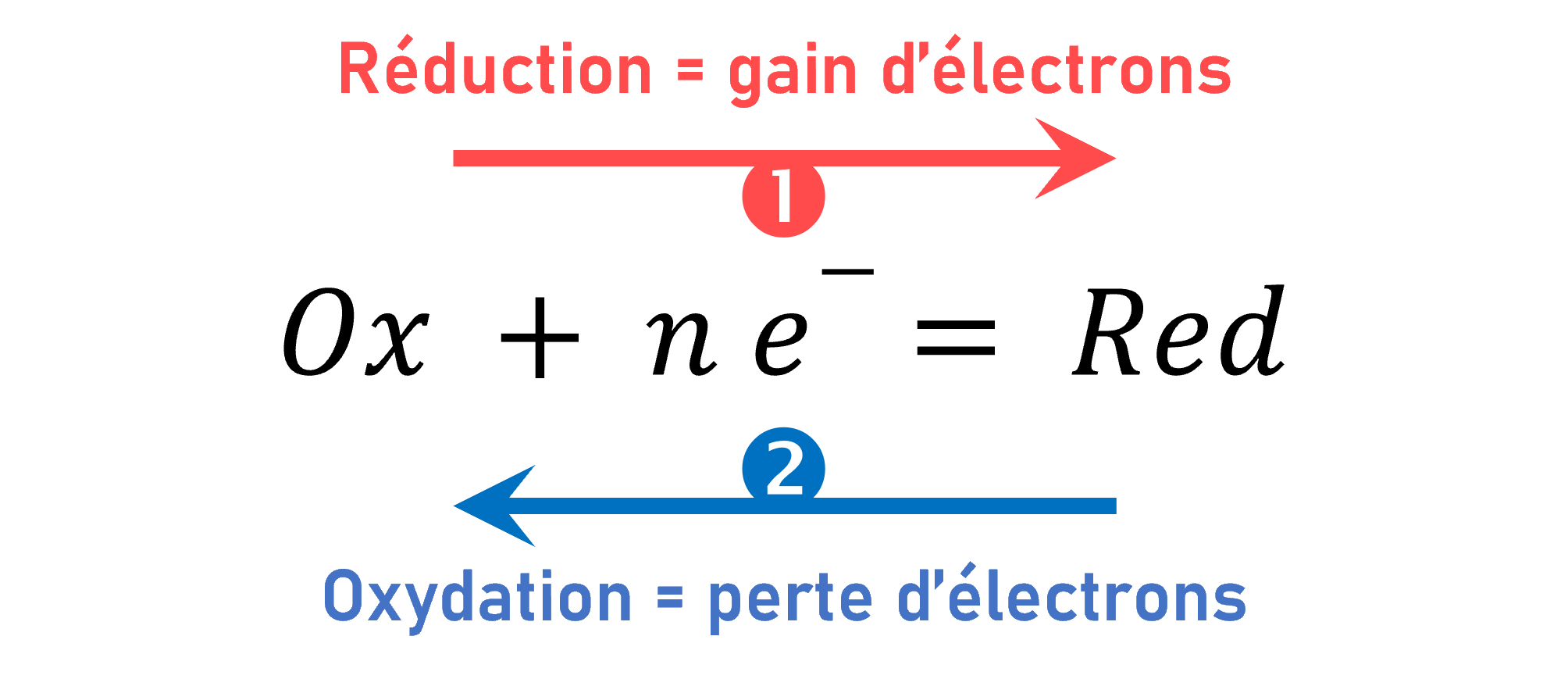
Si la demi-équation a lieu dans le sens 1️⃣ alors l’oxydant est réduit lors de la réaction de réduction.
Si la demi-équation a lieu dans le sens 2️⃣ alors le réducteur est oxydé lors de la réaction d’oxydation.
2. Comment écrire et ajuster une demi-équation électronique?⚓︎
Méthode pour écrie une demi-équation électronique :
1️⃣ Placer l’oxydant à gauche de la demi-équation et son réducteur conjugué à droite.
2️⃣ Equilibrer les éléments autres que l’oxygène et l’hydrogène.
3️⃣ Equilibrer si nécessaire l’élément oxygène en rajoutant des molécules d’eau \(H_2O(l)\), l’eau étant le solvant.
4️⃣ Equilibrer si nécessaire l’élément hydrogène en rajoutant des ions hydrogène \(H^+(aq)\).
5️⃣ Equilibrer les charges électriques en rajoutant des électrons, dans le membre de gauche.
3. Comment écrire une réaction d’oxydoréduction?⚓︎
Méthode pour écrire une réaction d’oxydoréduction :
1️⃣ Identifier les couples oxydant/réducteur des réactifs mis en jeu dans la réaction.
2️⃣ Etablir les demi-équations des couples oxydant/réducteurs mis en jeu.
3️⃣ Ecrire les 2 demi-équations afin que les 2 réactifs de la réaction soient dans le membre de gauche de chaque demi-équation.
4️⃣ Multiplier les demi-équations afin que les électrons s’annulent.
4. Exemple : réaction des ions iodure (\(I^-\)) avec les ions permanganate (\(MnO_4^-\))⚓︎
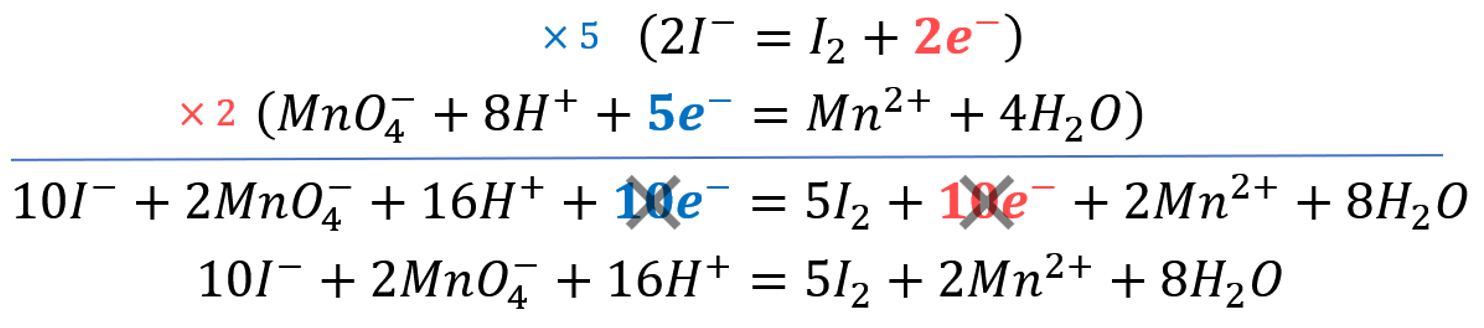
Rappels : Ajuster une équation chimique⚓︎
II - Evolution d'un système chimique⚓︎
A savoir
1. Avancement d'une réaction chimique⚓︎
L’avancement d’une réaction chimique, noté \(x\) et exprimé en moles (mol), est une grandeur qui permet de décrire l’évolution des quantités de matières d’un système chimique.
Il augmente depuis 0 mol dans l’état initial jusqu’à sa valeur finale \(x_f\), nommée avancement final, dans l’état final.
2. Avancement maximal et avancement final⚓︎
| Transformation totale | Transformation non totale |
|---|---|
| Transformation chimique qui s’arrête du fait de la consommation totale d’un de ses réactifs. | Transformation qui s’arrête alors que des réactifs n’ont pas été entièrement consommé |
| L’avancement final \(x_f\) est égal à une valeur maximale pour laquelle la quantité finale d’un des réactifs est nulle. Cette valeur est appelée avancement maximal et est notée \(x_{max}\) | l’avancement final \(x_f\) est alors inférieur à l’avancement maximal \(x_{max}\) |
| \(x_f=x_{max}\) | \(x_f<x_{max}\) |
3. Tableau d’avancement⚓︎
Le tableau d’avancement permet de calculer les quantités de matières des espèces chimiques d’un système chimique à tout moment de la réaction : il permet de faire un bilan de matière.
a) Détermination de l’état final pour une transformation totale⚓︎

Méthode pour remplir le tableau d'avancement
1️⃣ Pour chaque réactif, déterminer la valeur de \(x_{max}\) obtenue en supposant que ce réactif est le réactif limitant.
2️⃣ Comparer les valeurs obtenues : l’avancement maximal \(x_{max}\) est égal à la plus petite valeur trouvée.
3️⃣ La composition finale du système chimique s’obtient en remplaçant \(x_{max}\) par la plus petite valeur trouvée dans la dernière ligne du tableau d’avancement.
b) Détermination de l’état final pour une transformation non totale⚓︎
Lors d’une réaction non totale, il n’y a pas de réactif limitant : le système est composé des réactifs restants et des produits formés.
L’avancement final ne peut pas être calculé et il faut alors déterminer la quantité de matière finale de l’un des produits par un autre moyen (Par exemple dosage du mélange réactionnel au cours du temps) pour déterminer l’avancement final \(x_f\) et donc toutes les quantités de matière finales.
c) Cas particulier du mélange stœchiométrique⚓︎
On considère la réaction chimique \(a~A+b~B~=~c~C+d~D\)
Si à l'état initial on a \(\frac{n_i(A)}{a} = \frac{n_i(B)}{b}\) alors le mélange est dit stœchiométrique : tous les réactifs ont été introduits dans les proportions stœchiométriques, c’est-à-dire les proportions indiquées par l’équation de réaction.
Il n’y a alors pas de réactif en excès : pour une transformation totale, les quantités de matière finales de tous les réactifs sont donc nulles.